Vestibular
Classificação dos álcoois
Posição da hidroxila
Álcool primário: apresentam a hidroxila ligada a um carbono primário, ou seja, que se encontra ligado a apenas um outro átomo de carbono.
Exemplo:
CH3 ? OH
Metanol
Repare que a OH se encontra no extremo da cadeia e se liga apenas a um átomo de carbono.
Álcool secundário: apresentam a hidroxila ligada a um carbono secundário, ou seja, que se encontra ligado a outros dois átomos de carbono.
Exemplo:
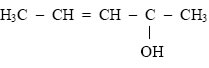
Penten-3-ol-2
Dizemos que o carbono é secundário quando está entre dois átomos de carbono.
Álcool terciário: apresentam a hidroxila ligada a um carbono terciário, ou seja, que se encontra ligado a outros três átomos de carbono.
Exemplo:
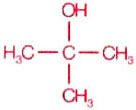
Metil-propanol-2
O carbono terciário se liga a outros três átomos de carbono.
Número de hidroxilas
Monoálcool: classificação dada a alcoóis que possuem apenas uma hidroxila ligada.
Exemplo:
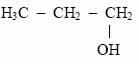
Propanol ? 1
Diálcool: álcool que possui duas hidroxilas ligadas à cadeia carbônica.
Exemplo:
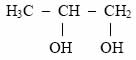
Propanodiol ? 1,2
Triálcool: este álcool conta com três hidroxilas em sua cadeia.
Exemplo:
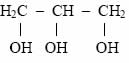
Propanotriol
Tipo de cadeia
Álcool de cadeia aberta: a cadeia que forma este álcool é linear, ou seja, não forma ângulos.
Exemplo:
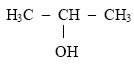
Propanol-2
Álcool de cadeia cíclica: a presença de uma figura geométrica caracteriza este tipo de álcool.
Exemplo:
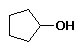
Ciclopentanol
Neste caso, a figura pentágono forma a estrutura carbônica.
Álcool de cadeia aromática: O álcool aromático possui um anel benzeno em sua estrutura.
Exemplo:
Fenol
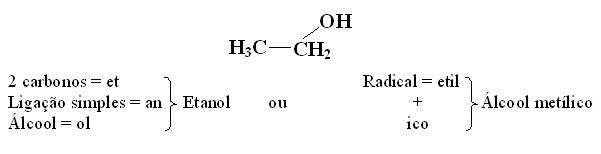
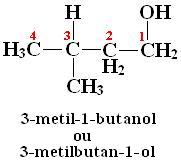
- Nomenclatura Dos Compostos Orgânicos
Nomeclatura dos compostos orgânicos Ontem eu fiz um post sobre as funções orgânicas e como prometido hoje vou comentar sobre a nomenclatura dos compostos orgânicos. O nome das estruturas orgânicas é dado por um prefixo (de acordo com um...
- Proteínas
1. O que são proteínas? Como a diversidade de proteínas nos seres vivos pode ser explicada? Proteínas são moléculas construídas por sequências de aminoácidos que se unem por ligações peptídicas. O código genético codifica vinte diferentes...
- Ácidos Carboxílicos, Cetonas, ésteres E éteres - Resumo (com Exercícios)
Ácidos carboxílicos Os ácidos carboxílicos são caracterizados pelo grupo carboxila (-COOH) , ligado à um carbono da cadeia principal. A fórmula estrutural plana da carboxila é: Esses compostos são ácidos fracos, mesmo...
- Nomenclatura Dos Hidrocarbonetos - Resumo (com Questões)
Nomenclatura dos hidrocarbonetos Os hidrocarbonetos são compostos orgânicos caracterizados por possuírem apenas átomos de carbono e hidrogênio. Conforme anteriormente, a nomenclatura dos compostos dessa função, que não apresentam ramificações...
- Classificação Das Cadeias Carbônicas - Resumo (com Questões)
CLASSIFICAÇÃO DAS CADEIAS CARBÔNICAS As cadeias carbônicas podem ser classificadas de acordo com quatro critérios fundamentais. Eles são: 1. Quanto ao fechamento da cadeia; 2. Disposição dos átomos dentro da cadeia; 3. Tipo de ligação...
Vestibular
Nomenclatura e classificação dos álcoois (com questões)
Artigo sobre classificação e nomenclatura dos álcoois com questões para um melhor aprendizado.
Função Álcool
Teremos um álcool quando um ou mais grupos hidroxila estiverem ligados diretamente a carbonos saturados, ou seja, que só fazem simples-ligação. O álcool mais simples estruturalmente é o metanol (H3COH), mas o mais importante economicamente é o etanol (álcool etílico).
Função Álcool
Teremos um álcool quando um ou mais grupos hidroxila estiverem ligados diretamente a carbonos saturados, ou seja, que só fazem simples-ligação. O álcool mais simples estruturalmente é o metanol (H3COH), mas o mais importante economicamente é o etanol (álcool etílico).
Classificação dos álcoois
Posição da hidroxila
Álcool primário: apresentam a hidroxila ligada a um carbono primário, ou seja, que se encontra ligado a apenas um outro átomo de carbono.
Exemplo:
CH3 ? OH
Metanol
Repare que a OH se encontra no extremo da cadeia e se liga apenas a um átomo de carbono.
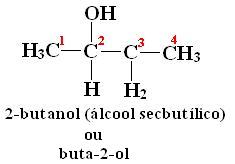
Álcool secundário: apresentam a hidroxila ligada a um carbono secundário, ou seja, que se encontra ligado a outros dois átomos de carbono.
Exemplo:
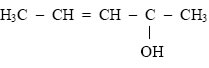
Penten-3-ol-2
Dizemos que o carbono é secundário quando está entre dois átomos de carbono.
Álcool terciário: apresentam a hidroxila ligada a um carbono terciário, ou seja, que se encontra ligado a outros três átomos de carbono.
Exemplo:

Metil-propanol-2
O carbono terciário se liga a outros três átomos de carbono.
Número de hidroxilas
Monoálcool: classificação dada a alcoóis que possuem apenas uma hidroxila ligada.
Exemplo:
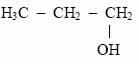
Propanol ? 1
Diálcool: álcool que possui duas hidroxilas ligadas à cadeia carbônica.
Exemplo:
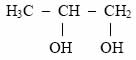
Propanodiol ? 1,2
Triálcool: este álcool conta com três hidroxilas em sua cadeia.
Exemplo:
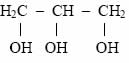
Propanotriol
Tipo de cadeia
Álcool de cadeia aberta: a cadeia que forma este álcool é linear, ou seja, não forma ângulos.
Exemplo:
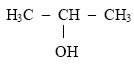
Propanol-2
Álcool de cadeia cíclica: a presença de uma figura geométrica caracteriza este tipo de álcool.
Exemplo:

Ciclopentanol
Neste caso, a figura pentágono forma a estrutura carbônica.
Álcool de cadeia aromática: O álcool aromático possui um anel benzeno em sua estrutura.
Exemplo:

Fenol
? Nomenclatura geral dos álcoois
Colocamos o prefixo indicador da quantidade de átomos de carbono (met, et, prop, etc), o infixo que indica o tipo de ligação (an, en, in) e o sufixo ?ol?, indicador da função álcoois.
Usualmente, os álcoois também são nominados a partir do nome do radical ligado à hidroxila mais o sufixo ?ico?.
Exemplo:
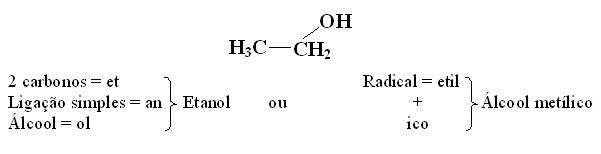
Quando o álcool tiver três ou mais átomos de carbono, devemos indicar a posição do grupo OH na cadeia. A numeração da cadeia começa sempre da extremidade mais próxima da hidroxila. Exemplo:
? Nomenclatura dos álcoois saturados com cadeia ramificada:
Caso o álcool tenha cadeia ramificada, teremos que indicar a posição e o nome da ramificação. Além disso, também devemos indicar a posição do grupo hidroxila.
O primeiro passo é encontrar a cadeia pricipal. Ela será aquela que apresentar maior número de carbonos e, neste caso, que contiver o grupo OH.
Feito isso, devemos numerar os átomos de carbono da cadeia principal, partindo sempre da extremidade mais próxima do grupo OH.
Por fim, basta dar nome ao composto, seguindo a seguinte ordem: número do carbono ao qual está ligado o radical, nome do radical e nome da cadeia principal. Exemplo:
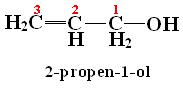
? Nomenclatura dos álcoois insaturados:
A dupla ligação é demonstrada pelo infixo ?en?, o grupo OH pelo sufixo ?ol? e a cadeia será numerada de forma que a hidroxila fique com o número mais baixo possível.
Neste caso, além de indicar a posição da hidroxila, também devemos indicar a posição da insaturação. O nome do composto será dado na seguinte ordem: posição da insaturação + hidrocarboneto correspondente + posição do OH + OL. Exemplo:
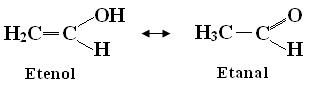
? Hidroxila ligada a carbono de dupla-ligação:
Neste caso, teremos outra função orgânica chamada ?enol?. Os enóis são quimicamente instáveis, pois a insaturação entre dois átomos de carbono é facilmente rompida, enquanto que a dupla ligação entre carbono e oxigênio é mais resistente. Devido a essa instabilidade, a dupla-ligação entre os carbonos pode migrar para a ligação entre o carbono e o oxigênio, formando cetona ou aldeído. No exemplo abaixo temos o ?etenol?, que, por sua instabilidade, coexiste em pequenas quantidades com o aldeído ?etanal?, mantendo um equilíbrio que chamamos de ?tautomerismo?:
Propriedades físicas dos álcoois
Os álcoois geralmente são líquidos (no máximo 10 carbonos no composto) ou sólidos (mais de 10 carbonos).
Solubilidade em água
A única parte polar dos álcoois é o grupo OH (hidroxila), por isso, quanto mais carbonos o álcool tiver, menor será a solubilidade, pois ?semelhante dissolve semelhante? (a água é polar).
Pontos de fusão e ebulição
Quanto maior for a cadeia do composto, maior será seu ponto de fusão e de ebulição.
O Etanol
O etanol é o mais importante dos álcoois, pois ele é um dos combustíveis que tem maior probabilidade de substituir o petróleo nas próximas décadas. É obtido através da fermentação de açúcares, como os presentes na cana-de-açúcar, milho, cevada, malte, etc, ou pela hidratação do etileno.
Além de ser misturado à gasolina (geralmente para baratear o preço), ele também é o álcool que está presente nas bebidas alcoólicas (daí o nome), como cerveja, vodka, cachaça e o absinto (bebida com o maior teor alcoólico, entre 45 e 85% de álcool, porém é feita uma destilação para que chegue à essa porcentagem). O que diferencia uma bebida da outra são as impurezas.
Seu ponto de fusão é de -114ºC, o que faz com que seja utilizado também como fluido para termômetros de temperaturas muito baixas (o mercúrio não serviria já que seu PF é de -40ºC).
Para se obter um etanol 100% puro, é preciso desidratar o acetaldeído, feito sinteticamente.
Exercícios sobre nomenclatura dos álcoois
a) b) c)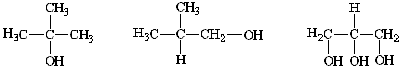
d) e)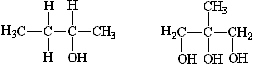
8) B
Fontes:http://www.labvirtq.fe.usp.br/simulacoes/quimica/sim_qui_nomenclaturadosalcoois.htm
http://www.infoescola.com/quimica/funcao-alcool/
Exercícios sobre nomenclatura dos álcoois
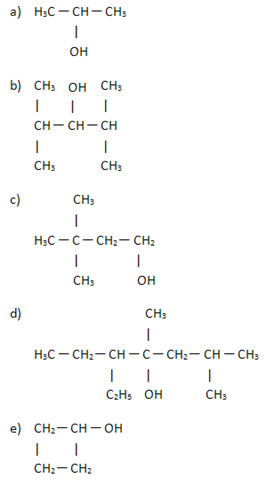
1) (FUVEST) O álcool terciobutílico é representado pela fórmula estrutural:
a) b) c)

d) e)
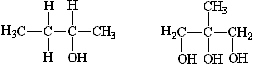
2) Dê os nomes, segundo as regras estabelecidas pela IUPAC (União Internacional de Química Pura e Aplicada), dos seguintes compostos:
4) Com se classificam os álcoois quanto à posição da hidroxila?
5) Como se classificam os álcoois quanto ao número de hidroxilas?
6) (UDESC 2010) Assinale a alternativa incorreta em relação aos alcoóis.
a) O etanol pode ser obtido a partir da reação do eteno na presença de água e ácido sulfúrico concentrado.
b) São compostos que apresentam o radical hidroxila ligado a carbono saturado.
c) O etanol, quando reage com dicromato de potássio em presença de ácido sulfúrico e com aquecimento, fornece o etanal como produto.
d) Em consequência da ponte de hidrogênio, os alcoóis possuem pontos de ebulição relativamente baixos.
e) A solubilidade dos alcoóis em água diminui gradativamente à medida que aumenta a cadeia carbônica, por causa da diminuição da polaridade.
7) (UDESC 2010) Considerando as funções orgânicas circuladas e numeradas presentes nas moléculas abaixo:
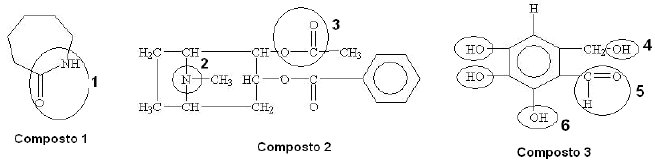
Assinale a alternativa correta.
a) No composto 3 a função orgânica circulada 4 representa um álcool.
b) No composto 1 a função orgânica circulada 1 representa uma amina.
c) No composto 2 a função orgânica circulada 3 representa um éter.
d) No composto 3 a função orgânica circulada 6 representa um álcool.
e) No composto 3 a função orgânica circulada 5 representa um ácido carboxílico.
8) (UFPB 2008)
Os químicos, com o objetivo de diminuir impactos negativos para o meio ambiente, têm produzido compostos sintéticos para usá-los como essências na produção de perfumes, substituindo os aromas naturais. Dentre esses compostos, encontram-se o MIRCENO, o CITRAL, o GERANIOL e a CIVETONA, conforme estruturas abaixo. Esses compostos substituem essências extraídas, respectivamente, da verbena, do limão, de rosas e de glândulas de um gato originário do Egito.
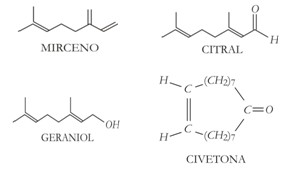
Em relação às estruturas desses compostos, é INCORRETO afirmar:
a) Civetona e Citral são compostos carbonílicos.
b) Geraniol é um álcool insaturado, com ligações duplas conjugadas.
c) Mirceno é um trieno que possui ligações duplas conjugadas.
d) Civetona possui cadeia cíclica, homogênea e insaturada.
e) Mirceno e Geraniol são, respectivamente, apolar e polar
4) álcool primário, secundário e terciário

3) Escreva as fórmulas estruturais e dê o nome oficial dos seguintes álcoois:
a) Álcool metílico
b) Álcool etílico
c) Álcool propílico
d) Álcool isopropílico
e) Álcool sec-butílico
f) Álcool terc-butílico
4) Com se classificam os álcoois quanto à posição da hidroxila?
5) Como se classificam os álcoois quanto ao número de hidroxilas?
6) (UDESC 2010) Assinale a alternativa incorreta em relação aos alcoóis.
a) O etanol pode ser obtido a partir da reação do eteno na presença de água e ácido sulfúrico concentrado.
b) São compostos que apresentam o radical hidroxila ligado a carbono saturado.
c) O etanol, quando reage com dicromato de potássio em presença de ácido sulfúrico e com aquecimento, fornece o etanal como produto.
d) Em consequência da ponte de hidrogênio, os alcoóis possuem pontos de ebulição relativamente baixos.
e) A solubilidade dos alcoóis em água diminui gradativamente à medida que aumenta a cadeia carbônica, por causa da diminuição da polaridade.
7) (UDESC 2010) Considerando as funções orgânicas circuladas e numeradas presentes nas moléculas abaixo:

Assinale a alternativa correta.
a) No composto 3 a função orgânica circulada 4 representa um álcool.
b) No composto 1 a função orgânica circulada 1 representa uma amina.
c) No composto 2 a função orgânica circulada 3 representa um éter.
d) No composto 3 a função orgânica circulada 6 representa um álcool.
e) No composto 3 a função orgânica circulada 5 representa um ácido carboxílico.
8) (UFPB 2008)
Os químicos, com o objetivo de diminuir impactos negativos para o meio ambiente, têm produzido compostos sintéticos para usá-los como essências na produção de perfumes, substituindo os aromas naturais. Dentre esses compostos, encontram-se o MIRCENO, o CITRAL, o GERANIOL e a CIVETONA, conforme estruturas abaixo. Esses compostos substituem essências extraídas, respectivamente, da verbena, do limão, de rosas e de glândulas de um gato originário do Egito.

Em relação às estruturas desses compostos, é INCORRETO afirmar:
a) Civetona e Citral são compostos carbonílicos.
b) Geraniol é um álcool insaturado, com ligações duplas conjugadas.
c) Mirceno é um trieno que possui ligações duplas conjugadas.
d) Civetona possui cadeia cíclica, homogênea e insaturada.
e) Mirceno e Geraniol são, respectivamente, apolar e polar
Gabarito:
1) A
2) a) Propan-2-ol
b) 2,4-dimetilpentan-3-ol
c) 3,3-dimetilbutan-1-ol
d) 5-etil-2,4-dimetil-heptan-4-ol
c) 3,3-dimetilbutan-1-ol
d) 5-etil-2,4-dimetil-heptan-4-ol
e) Ciclobutanol
3)

3)

4) álcool primário, secundário e terciário
5) Monoálcool, diálcool e triálcool.
6) D
7) A8) B
- Nomenclatura Dos Compostos Orgânicos
Nomeclatura dos compostos orgânicos Ontem eu fiz um post sobre as funções orgânicas e como prometido hoje vou comentar sobre a nomenclatura dos compostos orgânicos. O nome das estruturas orgânicas é dado por um prefixo (de acordo com um...
- Proteínas
1. O que são proteínas? Como a diversidade de proteínas nos seres vivos pode ser explicada? Proteínas são moléculas construídas por sequências de aminoácidos que se unem por ligações peptídicas. O código genético codifica vinte diferentes...
- Ácidos Carboxílicos, Cetonas, ésteres E éteres - Resumo (com Exercícios)
Ácidos carboxílicos Os ácidos carboxílicos são caracterizados pelo grupo carboxila (-COOH) , ligado à um carbono da cadeia principal. A fórmula estrutural plana da carboxila é: Esses compostos são ácidos fracos, mesmo...
- Nomenclatura Dos Hidrocarbonetos - Resumo (com Questões)
Nomenclatura dos hidrocarbonetos Os hidrocarbonetos são compostos orgânicos caracterizados por possuírem apenas átomos de carbono e hidrogênio. Conforme anteriormente, a nomenclatura dos compostos dessa função, que não apresentam ramificações...
- Classificação Das Cadeias Carbônicas - Resumo (com Questões)
CLASSIFICAÇÃO DAS CADEIAS CARBÔNICAS As cadeias carbônicas podem ser classificadas de acordo com quatro critérios fundamentais. Eles são: 1. Quanto ao fechamento da cadeia; 2. Disposição dos átomos dentro da cadeia; 3. Tipo de ligação...
